灵芝的医药价值无庸置疑,相关论文数量亦居所有食用菇之冠,灵芝原材料在中国的年产量也超过10万吨。如何从“产量大国”转型为“产值强国”,是所有灵芝业者念兹在兹的;如何从良莠不齐的灵芝产品中找到真正好的那一个,则是所有消费者和研究者深切关注的。由张劲松率领的上海市农业科学院食用菌研究所团队,2018年11月在第九届世界食用菌生物学与产品大会上的一系列报告,正是要告诉大家,“做好灵芝”不可或缺的要件。
文/吴亭瑶

张劲松(图中)和其团队研究员唐庆九(图右)丶冯娜(图左)丶刘艳芳等,分别通过〈影响灵芝产业发展关键鉴定方法和标准的研究〉丶〈灵芝有效成分的研究与质量标准的建立〉丶〈通过高效液相色谱技术建立灵芝三萜的一测多评方法〉丶〈灵芝β-葡聚糖的结构表徵丶生物活性研究及其定量检测方法开发〉等四场报告,解析如何建立准确的质控指标,助力做出好灵芝。(摄影/吴亭瑶)
张劲松开宗明义说道:如果“好灵芝”指的是“效果好的灵芝”,那么,决定灵芝好不好的关键,既非产地,也不是外观,而在它是否含有高生物活性成分。
研究显示,举凡品种(菌株)丶栽培模式(段木或袋栽)丶生长条件(光照丶温度丶湿度丶通气丶培养基)丶采收时机丶使用的灵芝部位(子实体丶孢子粉丶菌丝体),乃至当年的天候状况,都会影响灵芝的生物活性成分种类和含量。
换句话说,绝对不是任何名叫灵芝或看起来像灵芝的“灵芝”都有一样的生物活性成分(事实上有些根本不是灵芝),也不是哪个地方产的灵芝保证一定好或才算道地,外观长得漂不漂亮亦无以为据,更不可能野生放养会胜过人工栽培……
想要做出好灵芝的不二法门,只有使用好的品种,并且在标准化的栽培系统下控制所有生长条件,才能让每次种出来的灵芝,都稳定含有高生物活性成分;有了一批又一批含有高生物活性的原材料,才可能持续不断做出质量稳定丶功效卓着的好产品。
所以,为了把灵芝做好,我们需要DNA鉴定技术以确定和保证菌种来源的稳定,也需要通过育种技术培育出高孢子粉产量丶高三萜丶高多糖或其他特定需求的品种,同时亦需要针对灵芝里的主要活性成分建立“准确的”质量控制方法。
目前中国的灵芝企业几乎都是采用国家规定(由农业部制定)的灵芝三萜和多糖检测法作为产品的质量控制标准,其产品上标示的三萜丶多糖含量也都是按此方法检测的结果。
问题是,这个检测方法会受到外力严重干扰,像是:真正的灵芝三萜(如灵芝酸A丶灵芝酸B……)无法被测出来或严重低估,反而会把“不是灵芝三萜”的物质当作三萜来反映;又或者测到的多糖含量不只是灵芝多糖,连淀粉多糖丶糊精多糖都被一起算进来……
因此,在定性丶定量都不准的情况下,以中国国家规定的检测方法所测得的灵芝总三萜和总多糖,实际上和灵芝的生物活性并没有一定的相关性。
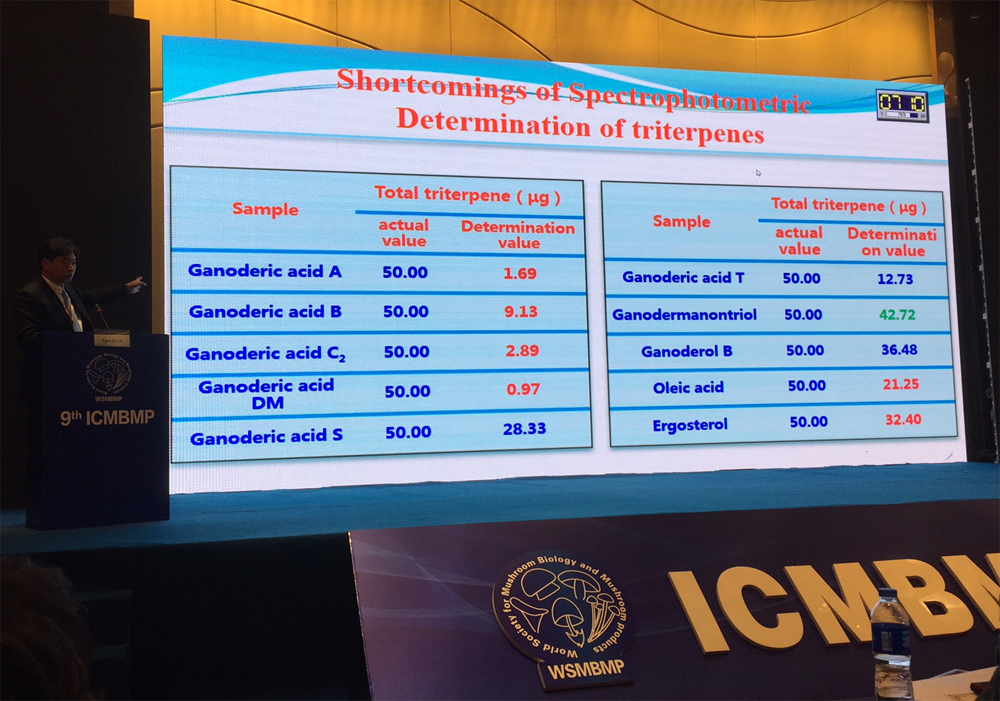
张劲松团队的研究发现,以中国农业部制定的灵芝三萜检测标准,对灵芝酸A(ganoderic acid A)丶灵芝酸B(ganoderic acid B)……等8种灵芝三萜标准品进行检测,并无法检测出其实际含量,反而会把“不是灵芝三萜”的油酸(oleic acid)和麦角甾醇(ergosterol)当作三萜来反映。(摄影/吴亭瑶,图为张劲松报告现场)
对此,张劲松特别强调,中国的灵芝企业按国家规定做事,在法理上一点错也没有,但企业如果真想做出好灵芝,就必须采用可以“真实反映”灵芝生物活性高低的检测方法作为内部的质控标准,才有办法保证自家产品的质量和功效。
能将混合物中的单一成分分离,并加以定性和量化各成分比例的HPLC(高效液相色谱法),向来是检测灵芝中各种活性成分的好方法。然而HPLC需要各种单一成分的标准品才能操作,在标准品取得不易和价格昂贵的现实考量下,令不少企业裹足不前。
为了解决这个问题,张劲松的团队已针对灵芝(Ganoderma lucidum)子实体中主要的活性多糖GLIS和17种活性三萜成分,开发出省钱丶方便又快速的检测方法。尤其对于三萜的“一测多评”,更是只要检测灵芝酸A(多数灵芝子实体中含量最高的三萜成分),即可通过对照的方式,对其他16种三萜做到绝对定量──精确得知各活性成分的含量非常重要,因为含量也会影响产品的功效表现。
只不过,不论是以活性多糖GLIS或灵芝酸A作为质控指标,都只适合用在以灵芝(Ganoderma lucidum)子实体为原料的产品,因为这两种活性成分“绝对不会”出现在孢子粉和菌丝体里。
因此,以孢子粉或菌丝体为原料的灵芝产品,乃至使用其他灵芝菌种(如紫芝Ganoderma sinense丶松杉灵芝Ganoderma tsugae),都必须根据原材料特有的活性成分,找出“对的”成分作为质控指标。至于检测方法,在经济实惠的方法被开发出来之前,HPLC可能还是比较理想的选择。
和“中国国家规定的灵芝三萜和多糖检测方法不准”一样令人难以面对的是,灵芝孢子里几乎不含三萜。
用“几乎”是科学的客观说法,因为大约十几二十吨的灵芝孢子粉,才能获得几克的三萜,比例之微小,已到了可以忽略不计的地步。而引发如此天大误会的源头,正是这个国家规定丶业界遵循的灵芝三萜检测法。
此方法制定于1990年代,当时离灵芝三萜被发现才短短几年,大家对于三萜的了解非常有限,拥有的技术也不如现在,以致用了错误的标准品(熊果酸或齐墩果酸,它们是植物萜类,而非灵芝特有的三萜)丶粗糙的检测方法(比色法,也称显色法),制定出一直被延用至今的灵芝三萜检测方法,所以才会在孢子粉,还有以孢子粉为原料进行提取的孢子油,验出根本不存在的灵芝三萜。
“但,没有三萜并不表示没有生物活性”,张劲松在报告时特别强调。已有许多实验证实孢子粉和孢子油具有抗肿瘤作用,只是为其带来抗肿瘤活性的成分并非三萜,而是麦角甾醇(ergosterol,也称麦角固醇)之类的甾醇(sterols,也称固醇)成分。
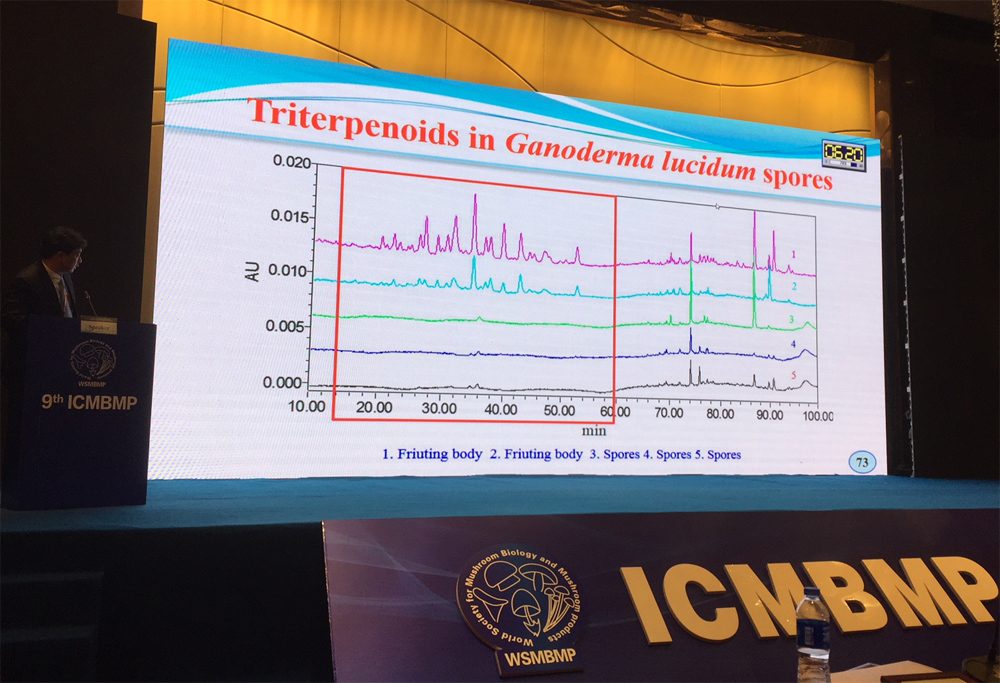
以HPLC法对Ganoderma lucidum子实体和孢子粉进行检测显示,两个不同来源的灵芝子实体里均含有多种三萜(曲线图上面两条曲线,每一个突起的峰就代表一种三萜成分),但三个不同来源的灵芝孢子粉都测不到三萜(曲线图下面三条曲线)。(摄影/吴亭瑶,图为张劲松报告现场)
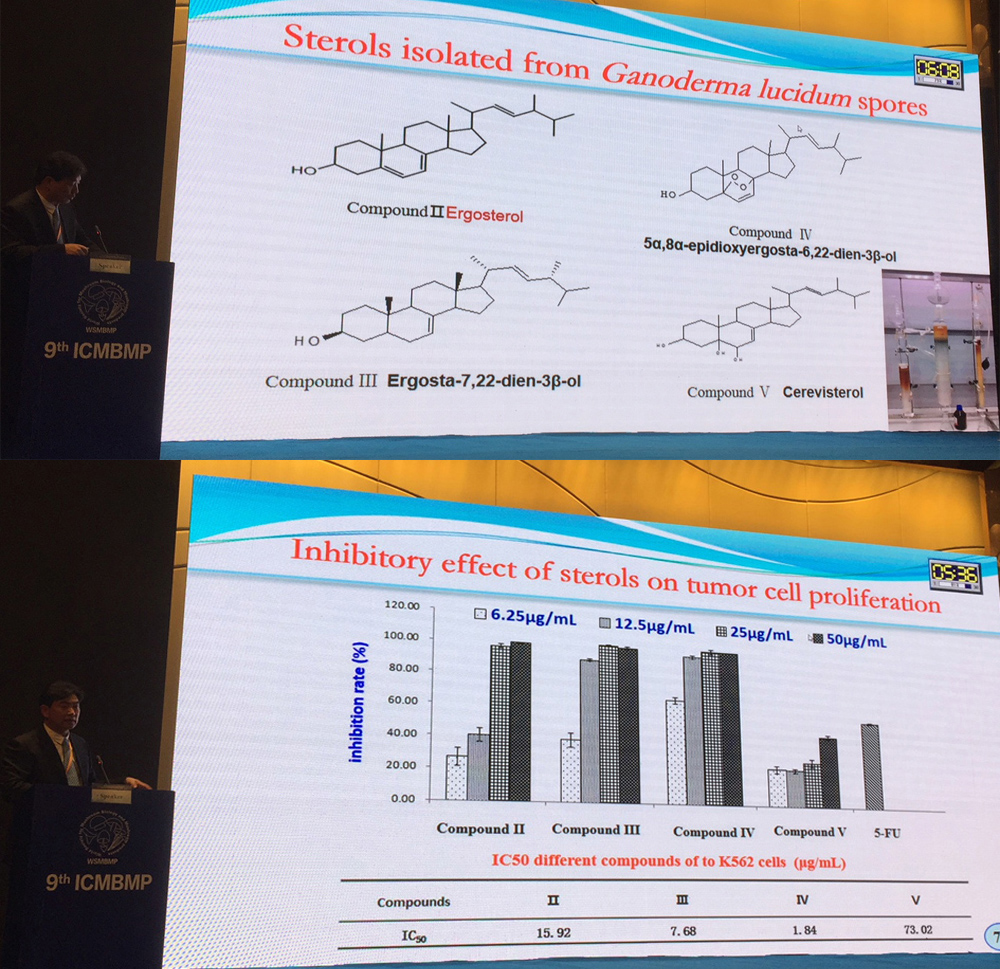
根据张劲松团队的研究显示,至少可从灵芝孢子粉中分离出四种甾醇成分(上图),它们对肿瘤细胞增生都有不等程度的抑制作用(下图)。(摄影/吴亭瑶,图为张劲松报告现场)
虽然结果都是抗肿瘤,但由于造成此结果的活性成分并非三萜,而是固醇,因此在栽种原材料和生产孢子粉丶孢子油的产品过程中,就该选择比较主要的固醇成分(如麦角甾醇)作为质控指标,才能确保质量和功效的稳定性。
孢子粉亦含有多糖(孢子的细胞壁组成就是多糖),所以也可以选择主要的多糖成分作为质控指标。只是来自孢子的多糖,和来自子实体的多糖,结构上完全不同,因此在选择质控指标时,不能张冠李戴,必须另外建立属于孢子粉的质控模式──这就像“鸡”和“鸡蛋”不同的道理,两者的质量监控指标怎会一样?
此外,张劲松在报告中也指出,孢子经过破壁后可大幅提高麦角固醇的获取量,因此对孢子粉丶孢子油产品来说,“破壁”是提高相关产品生物活性的重要技术。而在孢子油中占有很大比例的油酸成分,则值得多加探讨其对孢子油的功效有哪些贡献。
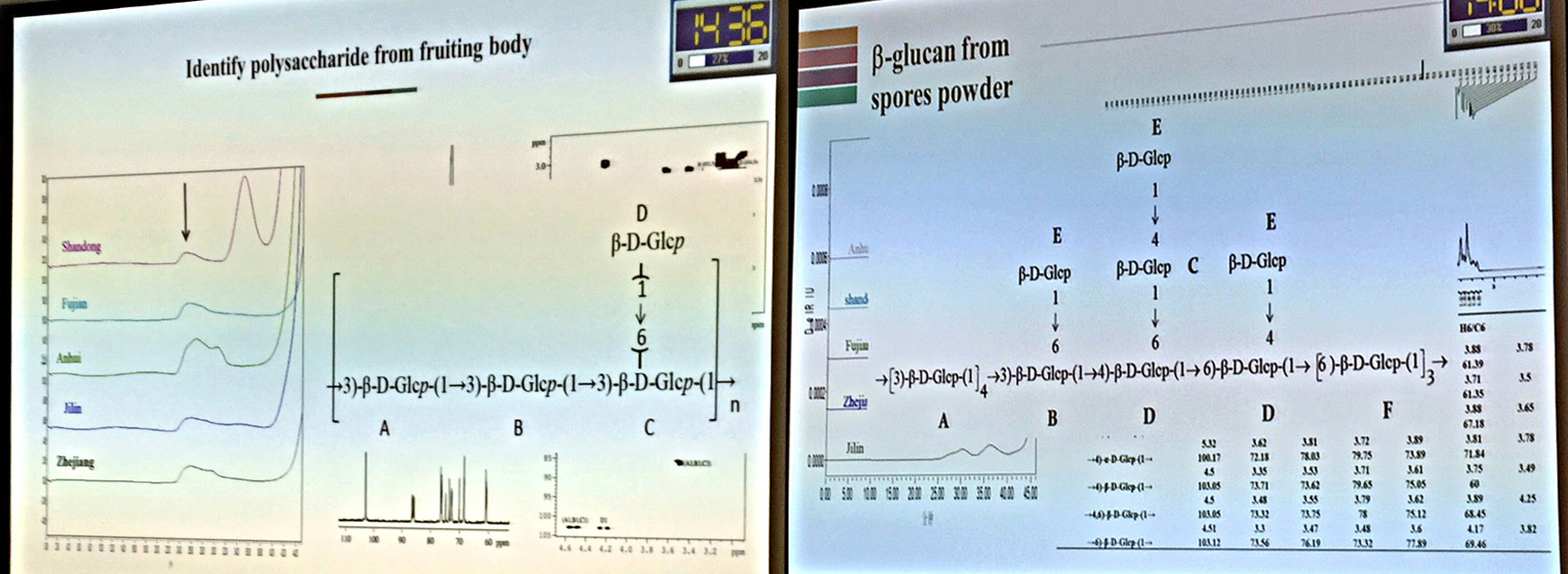
唐庆九在报告中明确指出,同样是灵芝Ganoderma lucidum,子实体来源的多糖(左图)和孢子粉来源的多糖(右图),化学结构组成明显不同。(摄影/吴亭瑶,图为唐庆九报告现场)

张劲松在报告中指出,三种不同来源的灵芝孢子粉,破壁前后测得的麦角甾醇含量有相当显著的差距,显示“破壁”是提高相关产品质量的重要技术。此外,在孢子油中占有很大比例的油酸,应被视为是孢子油的主要成分,值得多加探讨。(摄影/吴亭瑶,图为张劲松报告现场)
在“国家规定”没有改变的前提下,在中国销售的孢子粉丶孢子油产品,根据官方标准检测出来的三萜结果进行成分标示和文字宣传,是理所当然。
只是笔者以为,企业在行销的过程中,与其不断强调三萜与孢子粉丶孢子油的关系,甚或挪用子实体的三萜功效当作孢子粉丶孢子油的功效,还不如多与学界合作探讨甾醇或油酸成分的价值,多介绍真正的主角给消费者认识。当真正的活性成分足够强大时,一旦哪天没有三萜可以“借用”,消费者对于产品的信心也不致崩盘。
〔本文摘自:2018最重要的食用菌學術會議,討論了哪些重要的靈芝議題?──記第九屆世界食用菌生物學和產品大會(下)〕
COPYRIGHTS © Ganodermanews SINCE By 2015 ALL RIGHT RESERVED.
靈芝新聞網 版權所有 | 本網站內容作者享有其著作權,禁止侵害,違者必究
Powered by
ganodermanews.com