 生於1964年。現任中山醫學大學醫學研究所教授,專精毒理學、菇類免疫調節蛋白、癌症分子生物學和過敏之研究。
生於1964年。現任中山醫學大學醫學研究所教授,專精毒理學、菇類免疫調節蛋白、癌症分子生物學和過敏之研究。
1986年自輔仁大學生物學系畢業後,續留原系所攻讀碩士。1990年考入臺灣大學醫學院生化研究所,跟隨靈芝免疫調節蛋白的命名者,也是松杉靈芝免疫調節蛋白(FIP-gts)的發現者,林榮耀教授學習,並於1995年以其所發現之金針菇免疫調節蛋白為論文主題而取得博士學位。
爾後持續在免疫調節蛋白之路深耕,二十多年來對靈芝免疫調節蛋白抗過敏、抗肺癌作用的探究,尤其在肺癌細胞調控機制與協同化療作用的深入分析,已為靈芝免疫調節蛋白的應用開發打下穩固的根基。
更多介紹與著作詳見:中山醫學大學醫學研究所柯俊良教授。

中山醫學大學柯俊良教授團隊最新發表的研究顯示,對於已經對艾瑞莎或泰格莎產生抗藥性的肺腺癌細胞,小孢子靈芝免疫調節蛋白質GMI一方面能降低癌細胞的「別吃我」訊號CD47;另一方能面調整巨噬細胞的功能,促使免疫系統重新發揮清除能力。這種同時作用於「癌細胞訊號」與「免疫細胞功能」的雙重調控機制,為棘手的標靶抗藥性問題,提供了極具潛力的輔助免疫治療策略。
文/謝采穎 審定/辛翌綸、柯俊良

中山醫學大學柯俊良教授團隊2025年底發表的研究證明,不論EGFR雙突變的肺腺癌細胞是否已經對第三代標靶藥奧希替尼(泰格莎)產生抗藥性,GMI都能透過「促凋亡」和「促自噬」降低癌細胞的存活與增殖能力。柯教授提及本研究的起心動念是源於某次演講,有聽眾問起:「GMI對奧希替尼這個藥物會有影響嗎?在奧希替尼產生抗藥性之後還有幫助嗎?」才會發想本研究來進行探討,提供科學證據來證實GMI的功效。
文/吳亭瑤 審定/辛翌綸、柯俊良

中山醫學大學柯俊良教授研究靈芝免疫調節蛋白二十餘年,主要在探討以下幾個主題:(一) 抗過敏、抗發炎與免疫調節作用;(二) 抑制肺腺癌細胞的生長、轉移的能力與機制;(三) 對化療藥的輔助作用,包括減輕副作用、提升療效、降低癌細胞的抗藥性等。
整理/吳亭瑤
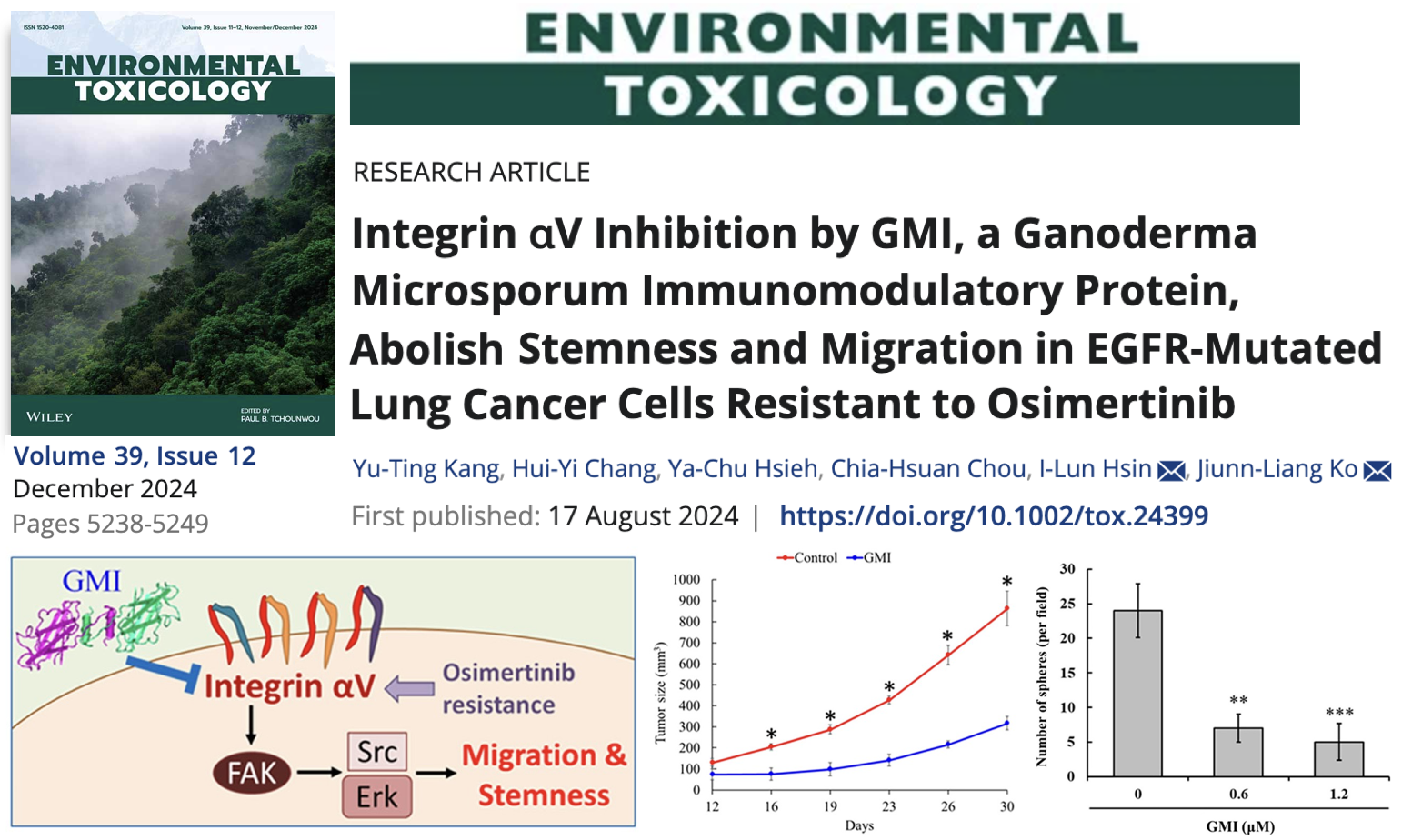
對於一再突變,甚至是一再對EGFR標靶藥出現抗藥性的突變型EGFR肺腺癌,只能換個標靶姿勢再治一次,還是走回傳統化療的老路?中山醫學大學醫學研究所柯俊良教授率其團隊成員辛翌綸博士、康于庭博士(台中榮民總醫院博士後研究員)等發表在2024年12月號《Environmental Toxicology》的研究讓我們看到了另一種因應的可能性,那就是既能顧前(清除EGFR)也能顧後(阻止癌細胞透過「整合素」另謀生路)的小孢子靈芝免疫調節蛋白質GMI(Ganoderma microsporum immunomodulatory protein)。
文/吳亭瑤

面對可能讓人瘦到皮包骨的惡病質,調節腸道微生物菌群被視為是沒有辦法中的辦法。向來是調節腸道菌群高手的靈芝,能夠阻止化療引發惡病質嗎?中山醫學大學醫學研究所柯俊良教授團隊今年五月發表的研究成果,首度給出肯定的答案。
文/吳亭瑤

今年4月由中山醫學大學附設醫院腫瘤內科主任吳銘芳醫師,以及中山醫學大學醫學研究所柯俊良教授等共同發表在《Medicine》的臨床研究發現,GMI口含片能在半個月內大幅修復頭頸癌患者的口腔黏膜炎,改善社交困難和體重減輕的問題,幫助患者能有較好的身心狀態進行下一輪化療。
文/吳亭瑤

可以被GMI助攻的抗癌搭擋又多了一個!今年七月柯俊良團隊發表在《Journal of Cellular Physiology》的論文證明,來自小孢靈芝的免疫調節蛋白GMI可以與口服劑型的Src酪胺酸激酶抑制劑「塞卡替尼(saracatinib)」發揮協同作用,提高對肺腺癌細胞的殺傷力,為GMI輔助癌症治療的科學證據再添一筆。
文/吳亭瑤
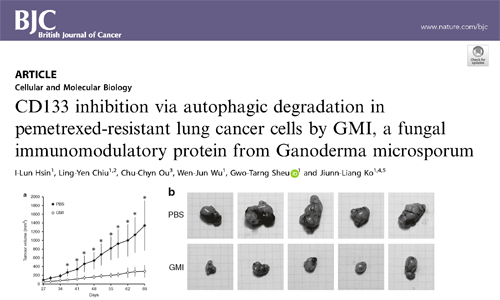
Pemetrexed(愛寧達注射劑)是治療肺腺癌的第一線化療藥,根據中山醫學大學醫學研究所柯俊良教授的團隊今年(2020)五月發表在《British Journal of Cancer》(英國癌症期刊)的研究證實,GMI可以刺激「具有Pemetrexed抗藥性的肺腺癌細胞」產生過度的自噬作用,讓癌細胞在自體吞噬的過程中自我了斷,不僅抑制腫瘤的生長,同時也把肺癌幹細胞一併處理了。
文/吳亭瑤

經科學證實有效的活性成分,在做成產品之後依然能被證實有效,才有能力給出「一定有效」的承諾。中山醫學大學醫學研究所柯俊良教授團隊剛發表在《Integrative Cancer Therapies》的報告即在證明,過去十年間被反覆證明具有多種免疫活性的小孢子靈芝免疫調節蛋白質GMI(Ganoderma microsporum immunomodulatory protein),在做成口含片劑型的膳食補充品(Reishimmune-S)之後,依然有效。
文/吳亭瑶

黑色素瘤是皮膚癌中最惡性的一種,一旦發展到快速生長期,很容易出現轉移,危及患者生命。小孢子靈芝免疫調節蛋白質GMI本身對黑色素瘤的增生和轉移就有很好的抑制效果,當它與臨床上用來治療皮膚癬、灰指甲、頭皮屑的Ketoconazole(酮康唑)聯手時,能對黑色素瘤細胞產生什麼樣的殺傷力呢?請看中山醫學大學蕭玉屏醫師與柯俊良教授團隊的研究成果。
文/吳亭瑶
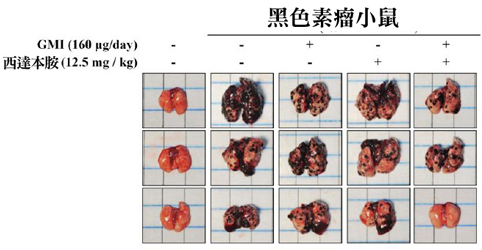
惡性黑色素瘤是皮膚癌中最危險的一種,一旦發生轉移,患者的存活率將大幅下降,因此,抑制癌細胞轉移就成了治療黑色素瘤的重要關鍵。中山醫學大學的研究證實,GMI不僅本身就對黑色素瘤細胞的移行能力有抑制作用,與新型標靶藥西達本胺併用時,不僅對癌細胞的存活與移行能力有更強的抑制作用,甚至還能抑制血管新生,切斷癌細胞的轉移路徑。動物實驗也證實,GMI+西達本胺對於抑制黑色素瘤遠端轉移有加乘效果。
文/吳亭瑤

2018年7月,中山醫學大學醫學研究所柯俊良教授的團隊在《Enviromnental Toxicology》發表了一篇報告證實,對於EGFR陽性的人類肺腺癌細胞,不管其EGFR是正常型或突變型,小孢子靈芝免疫調節蛋白質GMI都可通過抑制β-catenin表現量的方式,降低癌細胞的抗凋亡活性,把癌細胞推向窮途末路。這次的新發現,更加證明GMI這個由胺基酸組成的活性小分子蛋白,可以「多管齊下」制伏詭譎多變的肺腺癌。
文/吳亭瑶

中山醫學大學柯俊良教授和其團隊成員辛翌綸、邱彩醇等,發表在2016年12月《Phytomedicine(植物藥學)》的研究顯示,松杉靈芝(Ganoderma tsugae)免疫調節蛋白(簡稱FIP-gts)與氯奎寧(chloroquine,抗瘧疾藥物)併用,不管是對有抗藥性或沒抗藥性的人類泌尿道上皮癌細胞,都能有效抑制癌細胞的存活。
文/吳亭瑤

「細胞自噬」這個冷僻的專有名詞,因為日本學者大隅良典榮獲2016諾貝爾醫學獎而變得家喻戶曉。用如此高的殊榮來肯定他在基礎科學上的貢獻,不難想見瞭解細胞自噬這件事對於醫學發展有多重要。巧合的是,靈芝免疫調節蛋白的抗癌機制,主要就是來自細胞自噬作用的調控,其發現者正是中山醫學大學柯俊良教授所率領的研究團隊。
文/吳亭瑤
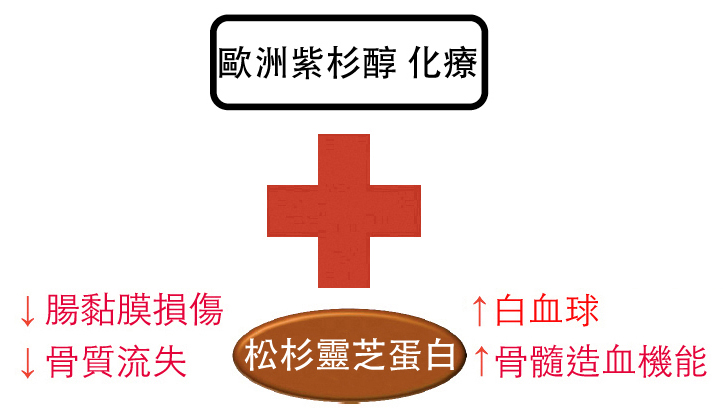
歐洲紫杉醇是廣泛應用於肺癌治療的化療藥劑,有很多副作用。而根據中山醫學大學柯俊良等的研究證實,來自松杉靈芝(Ganoderma tsugae)的免疫調節蛋白FIP-gts與歐洲紫杉醇併用,可顯著減輕白血球低下、小腸黏摸受損、骨質流失、骨髓造血機能抑制等不良反應,甚至能提升治療效果,降低轉移風險。
文/吳亭瑤 製圖/吳亭瑤、侯婷譯
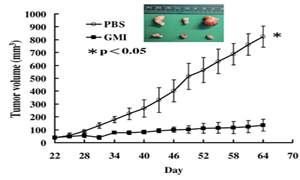
對多種藥物產生抗藥性(多重抗藥性),是癌症治療過程最不樂見的情況,尤其是治療困難度原本就很高的非小細胞肺癌。而根據中山醫學大學柯俊良教授的研究顯示,小孢子靈芝免疫調節蛋白質GMI,可以藉由阻斷Akt/mTOR訊息通路,迫使多重抗藥性的肺癌細胞自體吞噬,進而凋亡致死,為抗藥性肺癌的治療帶來希望。
文/吳亭瑤
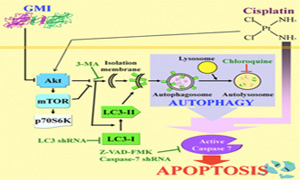
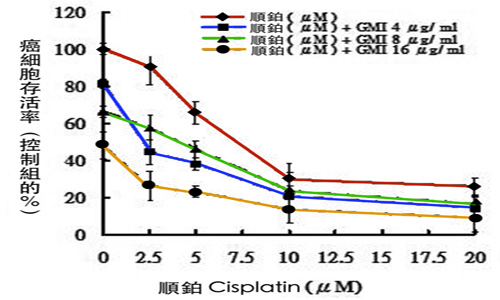
研究發現,把小孢子靈芝免疫調節蛋白質GMI和少量化療藥順鉑加在一起,可以讓大量非小細胞肺細胞凋亡。有趣的是,GMI本身促使肺癌細胞自噬的作用,並沒有因為順鉑的加入而受到影響,而且還反過來成為推動癌細胞凋亡的助力。
編譯/吳亭瑤

根據中山醫學大學醫學研究所柯俊良教授,以及台中榮總泌尿科醫師等人2014年發表在《Anticancer Research》的研究顯示,以松杉靈芝免疫調節蛋白FIP-gts處理「對順鉑有抗藥性」的泌尿道上皮癌細胞,可以降低癌細胞內beclin-1基因的表現,進而造成癌細胞自噬死亡,讓抗藥性的癌細胞不再抗藥。
文/吳亭瑤

「細胞自噬」是細胞在肌餓狀態下的自我保護機制,根據中山醫學大學醫學研究所柯俊良、辛翌綸等2011年發表在《Autophagy》的研究顯示,小孢子靈芝的免疫調節蛋白GMI可以促使肺癌細胞產生自噬而亡。由於過去許多化療藥物大多是以「促凋亡」作為主要的攻擊點,不少癌細胞已衍生出逃避凋亡機制的應對之道而產生抗藥性,因此誘發癌細胞自吞的抗癌方式,無疑是癌症治療的新利器。
文/吳亭瑤

容易轉移是肺癌不易治療的困難點之一,尤其是長期處在發炎狀態下,不只容易促進癌轉移的發生,更會造成肺部疾病的惡化。如何突破肺病難治的困境?根據中山醫學大學醫學研究所柯俊良教授團隊發表在美國化學學會官方刊物《Journal of Agricultural and Food Chemistry》的研究顯示,小孢子靈芝蛋白調節蛋白質GMI也許能為我們帶來希望──其作用機制不只有利肺癌的治療,還可能改善肺部發炎的相關疾病。
文/吳亭瑤

表皮生長因子EGF的刺激和EGFR的活化,是導致肺腺癌轉移的關鍵因素。中山醫學大學柯俊良教授、高雄醫學大學張建國教授等2010年發表在《Process Biochemistry》的研究即證實,小孢子靈芝免疫調節蛋白質GMI能在充斥EGF的環境下,阻止EGFR的活化,有效壓制肺腺癌細胞的轉移能力。
文/吳亭瑤
不同靈芝屬菌種皆含有一大約13 kDa分子量的蛋白質,具有免疫調節功能。根據本實驗室多年來的研究顯示,此類蛋白可以抑制肺癌細胞的端粒酶活性,促使肺癌細胞衰老和生長停滯。此外,靈芝免疫調節蛋白還能有效減緩上皮因子刺激癌細胞的轉移能力,並減少癌細胞本身的轉移和移行能力;與化療藥併用還能提高療效,提升白血球數量。
文.圖/柯俊良
Copyright © Ganodermanews.com since 2015. All rights reserved.
靈芝新聞網版權所有 | 本網站內容作者享有其著作權,禁止侵害違者必究