「細胞自噬」這個冷僻的專有名詞,因為日本學者大隅良典榮獲2016諾貝爾醫學獎而變得家喻戶曉。用如此高的殊榮來肯定他在基礎科學上的貢獻,不難想見瞭解細胞自噬這件事對於醫學發展有多重要。巧合的是,靈芝免疫調節蛋白的抗癌機制,主要就是來自細胞自噬作用的調控,其發現者正是中山醫學大學柯俊良教授所率領的研究團隊。
文/吳亭瑤
★敬請尊重著作權,歡迎以連結網址的方式友善分享,請註明作者、出處與圖片來源,並保留文章「從標題到參考文獻」的完整性,請勿將圖文移花接木、占為己有,或與商品、商業行為連結。
10月3日晚上七時許,當方念華主持的《Focus全球新聞》以最新消息發佈,日本東京工業大學教授大隅良典,因研究「細胞自噬」榮獲諾貝爾醫學獎時,原本吃飽想睡的我瞬間清醒,腦袋第一個想到的是「靈芝蛋白」與「柯俊良」。因為這位中山醫學大學醫學研究所教授,正是靈芝學界第一個證明「靈芝可在腫瘤動物體內透過『細胞自噬』作用抗癌」的學者,其所使用的材料正是靈芝裡特有的免疫調節蛋白(以下簡稱靈芝蛋白)。
聯絡上柯俊良時,電話那頭的他也難掩喜悅。原來他在2011年發表的第一篇靈芝蛋白促使肺腺癌細胞自噬死亡的研究,就有用到新科諾貝爾醫學獎得主提供的材料。雖然彼此間並不認識,僅用e-mail聯繫,大隅良典仍大方的無償予以協助,顯示其對細胞自噬相關研究有著一股純粹的熱情。一如中央社報導,大隅在獲獎後回應媒體,當初他之所以埋首研究細胞自噬的機制,並不是因為它未來有什麼用,純粹是「去發現沒人做的事,其實是很快樂的。」

什麼是「細胞自噬」?那是細胞在肌餓狀態下的自我保護機制,透過「自己吃自己」,吞噬細胞內比較不重要的細胞物質,再將它們進一步分解為養料(如:胺基酸或脂肪酸等小分子)重複利用來維繫生命。如果能適時獲得養分的補給,細胞就有機會存活下來;倘若一直等不到救援物資,細胞就會死亡。
早在1960年代就有人觀察到細胞的自噬現象,但直到1990年代大隅良典的研究和闡明,科學界才知道細胞內哪些基因的改變會引發細胞自噬,以及細胞內部「從自噬發生,到細胞死亡或存活的整個過程」會出現哪些變化。
也因為他打下的基礎,後面的科學家才會進一步發現,原來和癌症、自體免疫疾病(如類風濕性關節炎)、糖尿病、阿茲海默症等諸多疾病都與細胞自噬作用的失衡有關。如果能夠調控細胞自噬作用的機制,許多難治之症便有治癒的可能。
大隅良典帶來的醫療希望,正是諾貝爾醫學獎表揚他的原因;而用如此高的殊榮來肯定他的貢獻,不難想見「細胞自噬」這件事對於醫學發展有多重要。
如何針對不同疾病進行細胞自噬的調控,以達到治病效果,是近十年才開始熱門的研究議題。很多科學家都在找方法,而走在浪潮前端的柯俊良授則已多次證明,靈芝蛋白正是調控癌細胞自噬作用的高手。
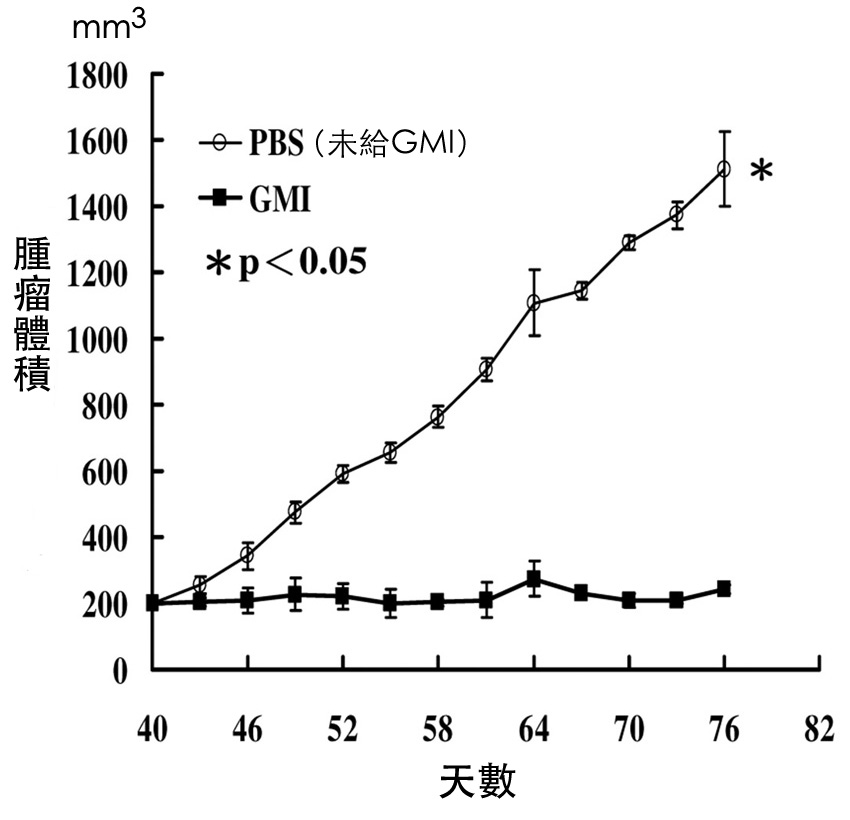
研究顯示,給植入肺癌細胞的裸鼠(免疫系統缺陷小鼠)餵食小孢子靈芝蛋白GMI,每天只要160 μg(=0.16 mg)的微小劑量,即可有效抑制腫瘤生長(圖1)。其腫瘤組織切片表現出顯著的細胞自噬反應,說明GMI正是透過此機制發揮抑瘤作用【1、2】。
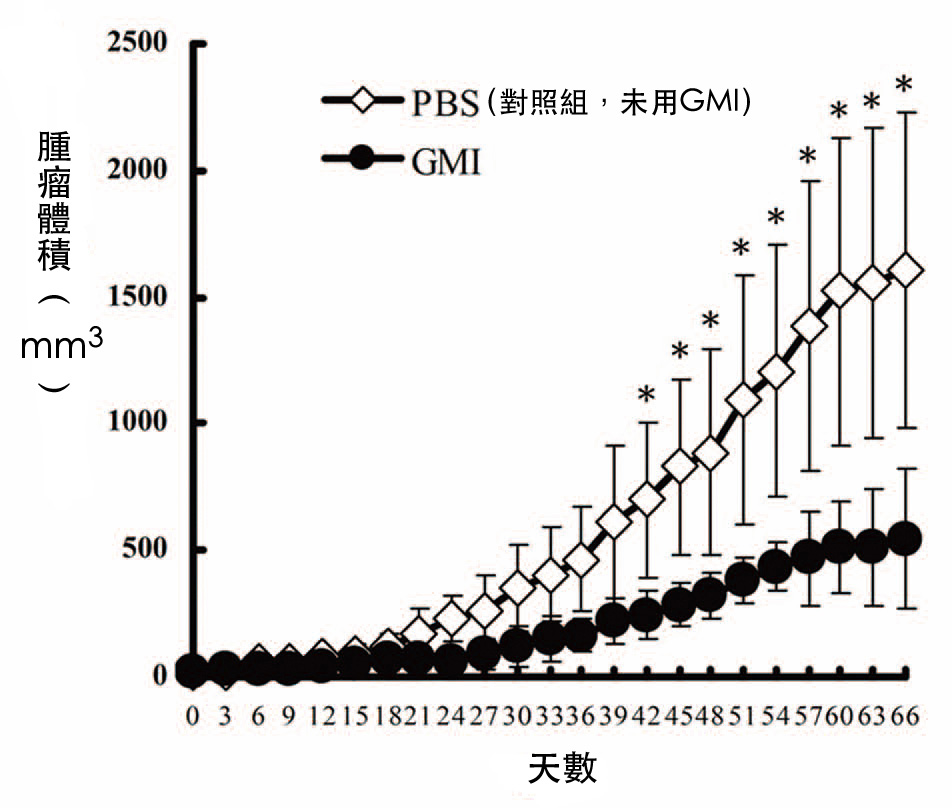
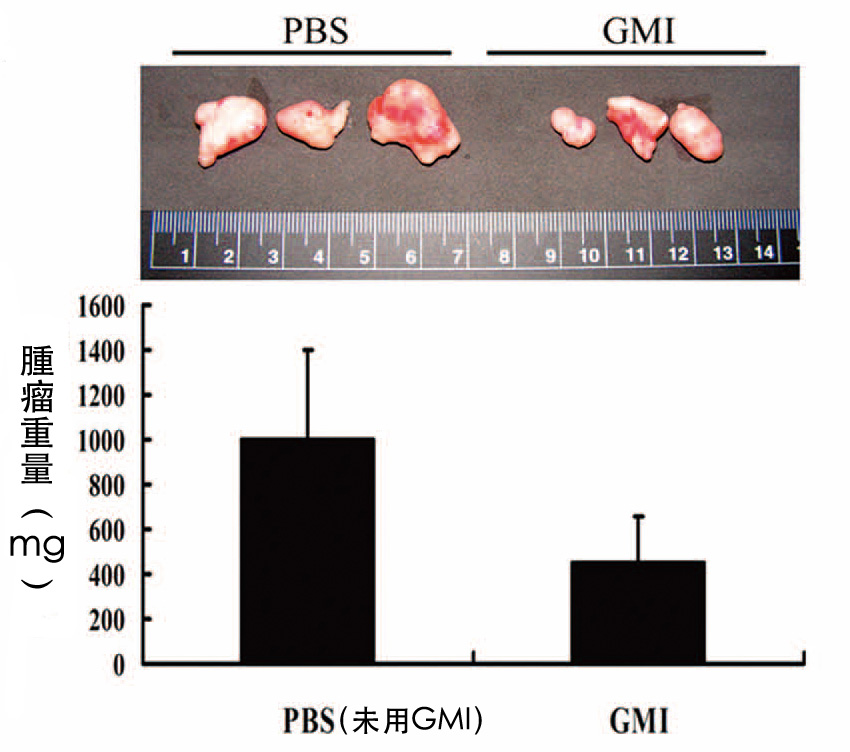
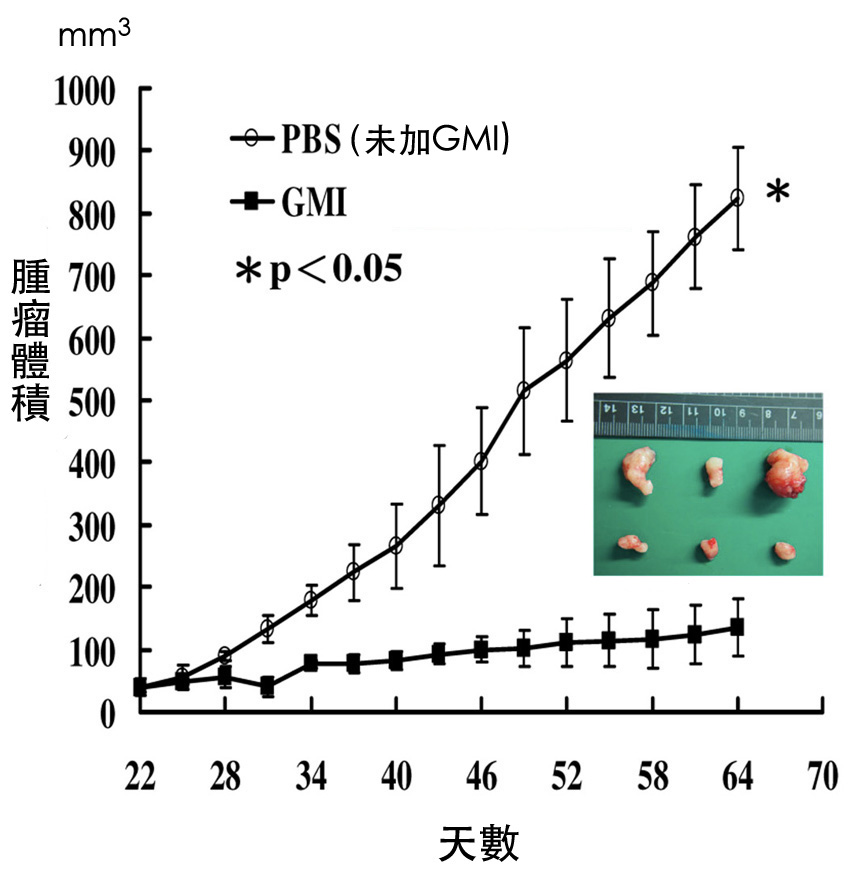
即使面對的是「具有抗藥性」的肺癌細胞, GMI同樣可以用160 μg的劑量在裸鼠體內發揮抑制腫瘤的作用,而且不管是在腫瘤還不明顯時就給GMI(圖2),或是等長出一定大小的腫瘤再給GMI(圖3),效果都很顯著,其主要的作用機制也和「加速癌細胞自噬死亡」有關【3】。
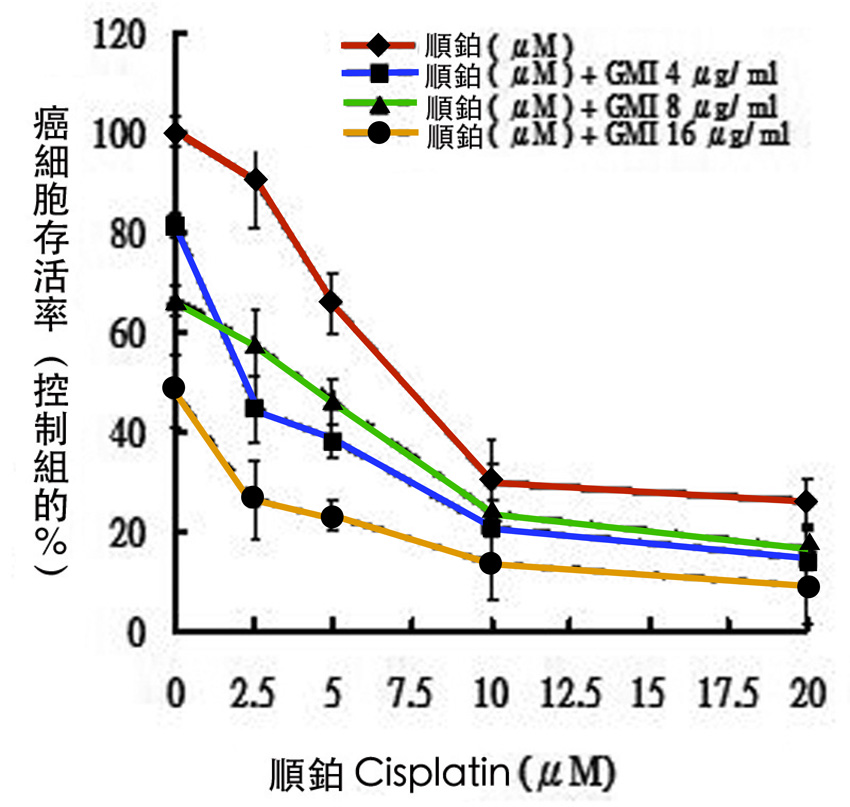
此外,細胞實驗也證實,不管GMI與順鉑(cisplatin)聯手對付一般的肺癌細胞,或與歐洲紫杉醇(docetaxel)聯手對付具「對歐洲紫杉醇有抗藥性」的肺癌細胞,都能通過細胞自噬作用,大幅提升癌細胞的死亡率(圖4)【3、4】。
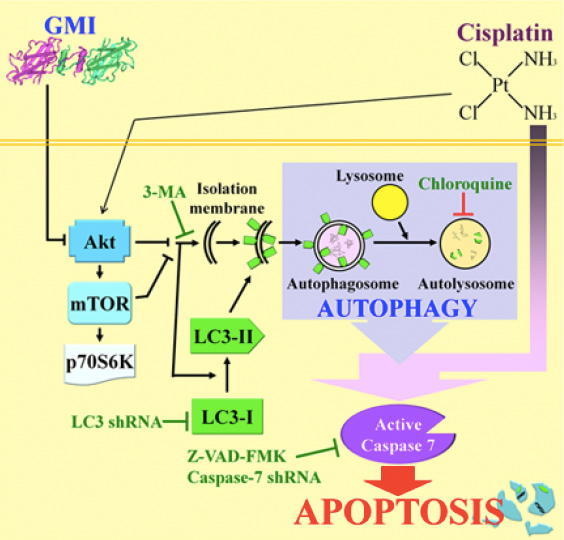
至於靈芝免疫調節蛋白到底調控了癌細胞內的哪些基因,活化了哪些蛋白分子,才讓肺癌細胞進入自噬狀態的,柯俊良的團隊也做了詳細的分析(圖5)【1~4】。
(資料來源/Mol Pharm. 2015. 12(5):1534-43.)
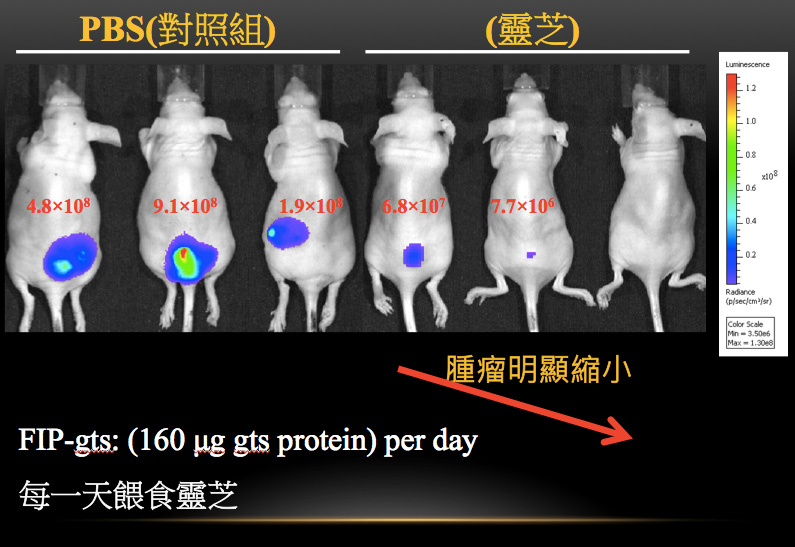
其實不只小孢子靈芝蛋白GMI有上述作用,柯俊良也曾用松杉靈芝蛋白FIP-gts做肺癌的動物實驗,雖然它和GMI的基因序列有17%的差異性,同樣也是只要每天給肺癌裸鼠口服160 μg的小劑量,就有類似GMI的抑瘤效果(圖6)。
除此之外,松杉靈芝蛋白FIP-gts也能啟動泌尿道上皮癌細胞(不管有沒有抗藥性)的自噬作用,加速癌細胞的死亡【5、6】。柯俊良表示,好發於男性的泌尿道上皮癌(膀胱癌的一種),目前標準的第一線治療藥是含有鉑金類的化療藥,一旦產生抗藥性,尚無標準的第二線化療藥可供使用,因此靈芝蛋白的效果很值得期待。
只是,如果促進癌細胞自噬,可以加速癌細胞死亡,那為什麼有些報導會說,「癌細胞為抵抗化療,會透過細胞自噬求生……少部分癌細胞無法被清除、出現抗藥性,推測與細胞自噬有關,將來若對癌症開發抑制細胞自噬藥物搭配化療使用,就有機會進一步清除頑強的癌細胞」,似乎與柯俊良的研究結果相衝突。
對此,柯俊良解釋,當癌細胞啟動自噬作用時,最後是生是死,要看它自噬到什麼程度,亦即癌細胞能否把它吃掉的部分進一步分解變成養分。有些癌細胞的分解能力很強,便可靠自噬作用求生,而出現所謂的抗藥性。因此如果有一種藥物可以調控細胞自噬過程的後半段,讓癌細胞無法分解吃掉的東西,那麼自噬到後來的結果,癌細胞本身反而會被撐破或毒死。這就是媒體報導上所說的,利用「抑制細胞自噬」讓癌細胞死亡的原理。
柯俊良說,其實靈芝蛋白既能透過基因調控,促使癌細胞出現自噬作用,也能阻止癌細胞在自噬過程中獲得養分,所以才能在體外實驗讓癌細胞死亡率大增,也才能在體內實驗讓裸鼠的腫瘤長不大──不管這腫瘤有沒有抗藥性,也不管靈芝蛋白有沒有與化療藥併用。
由於過去許多化療藥物大多是以「促凋亡」作為主要的攻擊點,不少癌細胞已衍生出逃避凋亡機制的應對之道而產生抗藥性,因此誘發癌細胞自吞的抗癌方式,無疑是癌症治療的新利器。
不過更為柯俊良稱道的是,靈芝蛋白還可保護正常細胞,減輕化療藥的傷害。去年(2015)發表的報告即證實,松杉靈芝蛋白FIP-gts減輕歐洲紫杉醇引發的多種副作用【7、8】。
歐洲紫杉醇常用於肺癌、乳癌的治療,如果能將靈芝蛋白開發成臨床用藥,將造福多少病友啊!最重要的是,根據已經完成的毒理評估顯示,靈芝蛋白的安全性很高,而且靈芝蛋白是單一成分,化學結構與基因序列也都完全清楚,還能進行大規模的工業化量產,所以現在只差做出更多的臨床和機制研究,就有機會讓癌症多一個治療的希望。
研究靈芝蛋白超過二十年的柯俊良說,實在想不到一個小小的蛋白,有這麼多的作用。其實自從他發表靈芝蛋白和癌細胞自噬相關的論文後,許多靈芝研究團隊也開始朝這個方向探討。他們有的用不同來源的靈芝蛋白(如LZ-8、FIP-gat),有的用三萜類總萃取物、靈芝酸或赤芝酸,討論的作用也鎖定在抗腫瘤作用。有這麼多不同的研究團隊和他有志一同,實在始料未及。
想當初,柯俊良之以會注意到靈芝蛋白與細胞自噬的關係,主要是因為靈芝蛋白對肺癌細胞的促凋亡作用很微弱,「但奇怪的是,那些因為癌細胞在出現衰老狀態之後,經過一段較長的時間還是會死,所以才會想到,可能是『細胞自噬』這個機制。」只是為什麼原本長生不老的癌細胞會「衰老」?原來是靈芝蛋白阻斷了癌細胞永保青春的源頭──抑制癌細胞染色體的端粒酶活性。
「真的很巧,我研究細胞自噬沒多久,大隅良典就因細胞自噬研究而獲得諾貝爾醫學獎;之前我研究端粒酶活性也是,也是研究結果出來沒幾年,就有學者因為研究端粒酶而獲得諾貝爾醫學獎。」果真如此,2009年的諾貝爾醫學獎正是頒給三位「發現端粒和端粒酶如何保護染色體」的科學家,而柯俊良發表第一篇「靈芝蛋抑制肺癌細胞端粒酶活性」論文的年份則是2006年【9】。
哇~柯老師,您會預言嗎?下回您要研究靈芝蛋白的什麼作用,來讓我們大開眼界?也許未來幾年的諾貝爾醫學獎評審團,又會和您英雄所見略同呢!
1. Hsin IL, et al. GMI, an immunomodulatory protein from Ganoderma microsporum, induces autophagy in non-small cell lung cancer cells. Autophagy. 2011 Aug 1;7(8):873-82.
2. Hsin IL, et al. Inhibition of lysosome degradation on autophagosome formation and responses to GMI, an immunomodulatory protein from Ganoderma microsporum. Br J Pharmacol. 2012 Nov;167(6):1287-300. doi: 10.1111/j.1476-5381.2012.02073.x.
3. Chiu LY, et al. Immunomodulatory protein from Ganoderma microsporum induces pro-death autophagy through Akt-mTOR-p70S6K pathway inhibition in multidrug resistant lung cancer cells. PLoS One. 2015 May 6;10(5):e0125774. doi: 10.1371/journal.pone.0125774. eCollection 2015.
4. Hsin IL, et al. GMI, an immunomodulatory protein from Ganoderma microsporum, potentiates cisplatin-induced apoptosis via autophagy in lung cancer cells. Mol Pharm. 2015. 12(5):1534-43. doi: 10.1021/mp500840z.
5. Li JR, et al. FIP-gts potentiate autophagic cell death against cisplatin-resistant urothelial cancer cells. Anticancer Res. 2014 Jun;34(6):2973-83.
6. Hsin IL, et al. Immunomodulatory proteins FIP-gts and chloroquine induce caspase-independent cell death via autophagy for resensitizing cisplatin-resistant urothelial cancer cells. Phytomedicine. Available online 10 September 2016. doi: 10.1016/j.phymed.2016.09.003.
7. Ou CC, et al. Fungal immunomodulatory proteins alleviate docetaxel-induced adverse effects. Journal of Functional Foods. 2015 Sep; 19: 451-463.
8. 侯婷譯,探討真菌類免疫調節蛋白質改善歐洲紫杉醇引起的不良副作用。中山醫學大學醫學研究所碩士論文,2014。
9. Liao CH, et al. Transcriptionally mediated inhibition of telomerase of fungal immunomodulatory protein from Ganoderma tsugae in A549 human lung adenocarcinoma cell line. Mol Carcinog; 2006. 45(4):220-9.
Copyright © Ganodermanews.com since 2015. All rights reserved.
靈芝新聞網 版權所有 | 本網站內容作者享有其著作權,禁止侵害,違者必究